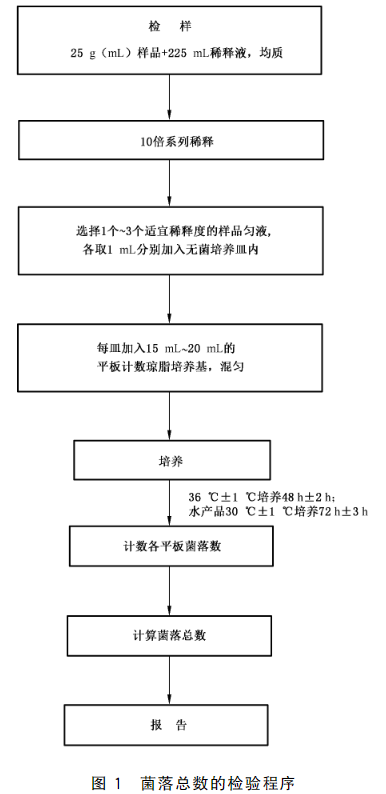
食品检样经过处理,在一定条件下培养后(如培养基成分、培养温度和时间、pH、需氧性质等),所得1mL(或1g)检样中形成菌落的总数。
按国家标准方法规定,即在需氧情况下,37℃培养48h,能在平板计数琼脂平板上生长的细菌菌落总数,所以厌氧或微需氧菌、有特殊营养要求的以及非嗜中温的细菌,由于现有条件不能满足其生理需求,故难以繁殖生长。因此菌落总数并不表示实际中的所有细菌总数,菌落总数并不能区分其中细菌的种类,所以有时被称为杂菌数,需氧菌数等。
细菌总数指一定数量或面积的食品样品.经过适当的处理后,在显微镜下对细菌进行直接计数。其中包括各种活菌数和尚未消失的死菌数。细菌总数也称细菌直接显微镜数。通常以1g或1mL或1cm2样品中的细菌总数来表示。

1、食品中细菌数量可反映该食品被污染的程度
新鲜的食品内部一般是没有或很少有细菌的,但由于外界污染情况不同,食品被细菌污染的多少就有所不同。食品中细菌数量越多,说明被污染的程度就越严重,越不新鲜,对人体健康威胁越大。相反,食品中菌数越少,说明该食品被污染的程度越轻,食品卫生质量越好,对人体健康影响也越小。
2、食品中细菌数量可预测食品耐放程度和时间
一般讲,细菌数越少,食品耐放时间越长;相反,食品耐放时间就越短,例如用0℃保存牛肉,菌落总数为l03CFU/cm2时,可保存18天,而当菌落总数增至l05CFU/cm2时则只能保存7天。另外,用0℃保存鱼时,菌落总数为l05CFU/cm2时可保存6天。而菌落总数在l03CFU/cm2时则可保存12天。
3、食品中细菌数量可估测出食品腐败状况
一般认为日常食品的活菌数为l04~l07CFU/g。而当活菌数达到l08CFU/g则可认为处于初期腐败阶段。例如,活的家禽,皮肤表面的细菌数可低到1.5×l03CFU/cm2。而加工后马上检测可达3.5×l04CFU/cm2。当菌落数为l07CFU/cm2时表示确已经腐败,鸡肉的细菌数达l08CFU/cm2时可有气味并变粘。
一般讲,食品中细菌数量越多,则会加速腐败变质过程的进程,甚至可能引起食用者的不良反应。
菌落总数检测方法
菌落总数的常规检验方法菌落总数的常规检验方法(GB4789.2-2022)。
基本操作一般包括:样品的稀释——倾注平皿——培养48(72)小时——计数报告。
1、操作方法
(1)以无菌操作取检样25g(或25mL),放于225mL无菌生理盐水或其他无菌缓冲溶液的无菌锥形瓶(瓶内预置适当数量的玻璃珠)或无菌均质袋内,经充分振要或研磨制成1:10的均匀稀释液。
固体检样在加入稀释液后,最好置灭菌均质器中以8000~10000r/min的速度处理1~2min,制成1:10的均匀稀释液。
(2)用1ml灭菌吸管或吸头吸取1:10稀释液1mL,沿管壁徐徐注入含有9mL灭菌生理盐水或其他稀释液的无菌试管内,振摇试管混合均匀,制成1:100的稀释液。
(3)另取1mL灭菌吸管或吸头,按上项操作顺序,制10倍递增稀释液,如此每递增稀释一次即换用1支1mL灭菌吸管。
2、无菌操作
操作中必须有“无菌操作”的概念,所用玻璃器皿必须是完全灭菌的。所用剪刀、镊子等器具也必须进行消毒处理。样品如果有包装,应用75%乙醇在包装开口处擦拭后取样。
操作应当在超净工作台或经过消毒处理的无菌室进行。琼脂平板在工作台暴露15分钟,每个平板不得超过5个菌落(具体的自己根据实际制定实验室的SOP)。
3、采样的代表性
如系固体样品,取样时不应集中一点,宜多采几个部位。固体样品必须经过均质或研磨,液体样品须经过振摇,以获得均匀稀释液。
4、稀释液
样品稀释液主要是灭菌生理盐水,有的采用磷酸盐缓冲液(或0.1%蛋白胨水),后者对食品已受损伤的细菌细胞有一定的保护作用。如对含盐量较高的食品(如酱油)进行稀释,可以采用灭菌蒸馏水。
1、操作方法
(1)根据标准要求或对污染情况的估计,选择1~3个适宜稀释度,分别在制10倍递增稀释的同时,以吸取该稀释度的吸管移取1mL稀释液于灭菌平皿中,每个稀释度做两个平皿。
(2)将凉至46℃~50℃平板计数琼脂培养基注入平皿约15~20mL,并转动平皿,混合均匀。同时将平板计数琼脂培养基倾入加有1mL稀释液(不含样品)的灭菌平皿内作空白对照。
(3)待琼脂凝固后,翻转平板,置36±1℃温箱内培养48±2h,取出计算平板内菌落数目,乘以稀释倍数,即得每克(每毫升)样品所含菌落总数。
(4)倾注用培养基应在48℃±2℃水浴内保温,温度过高会影响细菌生长,过低琼脂易于凝因而不能与菌液充分混匀。如无水浴,也可以以皮肤感受较热而不烫为宜。
倾注培养基的量规定不一,从12~20mL不等,一般以15mL较为适宜,平板过厚可影响观察,太薄又易于干裂。倾注时,培基底部如有沉淀物,应将底部弃去,以免与菌落混淆而影响计数观察
(5)为使菌落能在平板上均匀分布,检液加入平皿后,应尽快倾注培养基并旋转混匀,可正反两个方向旋转,检样从开始稀释到倾注最后一个平皿所用时间不宜超过20min,以防止细菌有所死亡或繁殖。
(6)一般适温较低,故多采用36℃,培养时间一般为48h。培养箱应保持一定的湿度,琼脂平板培养48h后,培养基失重不应超过15%。
(7)为了避免食品中的微小颗粒或培基中的杂质与细菌菌落发生混淆,不易分辨,可同时作一稀释液与琼脂培养基混合的平板,不经培养,而于4℃环境中放置,以便计数时作对照观察。
在某些时候,为了防止食品颗粒与菌落混淆不清,可在营养琼脂中加入氯化三苯四氮唑(TTC),培养后菌落呈红色,易于分别。
培养到时间后,计数每个平板上的菌落数。可用肉眼观察,必要时用放大镜检查,以防遗漏。在记下各平板的菌落总数后,求出同稀释度的各平板平均菌落数,计算出原始样品中每克(或每mL)中的菌落数,进行报告。
2、计数
到达规定培养时间,应立即计数。如果不能立即计数,应将平板放置于0-4℃,但不得超过24h。
3、稀释度选择及菌落数报告方式
(1)若只有一个稀释度平板上的菌落数在适宜计数范围内,计算两个平板菌落数的平均值,再将平均值乘以相应稀释倍数,作为每克(或毫升)中菌落总数结果。
(2)若有两个连续稀释度的平板菌落数在适宜计数范围内时,按式(l)计算:
N=∑C/(n1+0.1n2)d……………………(1)
式中:
N―样品中菌落数;
∑C―平板(含适宜范围菌落数的平板)菌落数之和;
n 1―第一个适宜稀释度接种平板个数
n2―第二个适宜稀释度接种平板个数;
d―稀释因子(第一稀释度)。
(3)若所有稀释度的平板上菌落数均大于300,则对稀释度最高的平板进行计数,其他平板可记录为多不可计,结果按平均菌落数乘以最高稀释倍数计算。
(4)若所有稀释度的平板菌落数均小于30,则应按稀释度最低的平均菌落数乘以稀释倍数计算。
(5)若所有稀释度(包括液体样品原液)平板均无菌落生长,则以小于1乘以最低稀释倍数计算。
(6)若所有稀释度的平板菌落数均不在30~300之间,其中一部分小于30或大于300时,则以最接近30或300的平均菌落数乘以稀释倍数计算。
4、菌落总数的报告
(1)菌落数在100以内时,按“四舍五人”原则修约,采用两位有效数字报告。
(2)大于或等于100时,第三位数字采用“四舍五人”原则修约后,取前两位数字,后面用0代替位数;也可用10的指数形式来表示,按“四舍五入”原则修约后,采用两位有效数字。
(3)若空白对照上有菌落生长,则此次检测结果无效。
(4)称重取样以CFU/g为单位报告,体积取样以CFU/mL 为单位报告。
1、不同稀释度的菌落数应与稀释倍数成反比(同一稀释度的二个平板的菌落数应基本接近),即稀释倍数愈高菌落数愈少,稀释倍数愈低菌落数愈多。如出现逆反现象,则应视为检验中的差错(有的食品有时可能出现逆反现象,如酸性饮料等),不应作为检样计数报告的依据。
2、当平板上有链状菌落生长时,如呈链状生长的菌落之间无任何明显界限,则应作为一个菌落计,如存在有几条不同来源的链,则每条链均应按一个菌落计算,不要把链上生长的每一个菌落分开计数。如有片状菌落生长,该平板一般不宜采用,如片状菌落不到平板一半,而另一半又分布均匀,则可以半个平板的菌落数乘2代表全平板的菌落数。
3、当计数平板内的菌落数过多(即所有稀释度均大于300时),但分布很均匀,可取平板的一半或1/4计数。再乘以相应稀释倍数作为该平板的菌落数。